高考化学卷中,有机化学通常占据 15% – 20% 左右的分值。无论是选择题还是必做的有机推断大题,其本质都是在考查“结构决定性质,性质反映结构”这一核心思想。
常见官能团的结构与性质
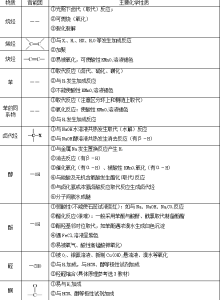
根据常见试剂或特征现象
推断官能团种类
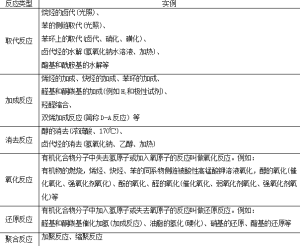
常见的有机反应类型

高考化学卷中,有机化学通常占据 15% – 20% 左右的分值。无论是选择题还是必做的有机推断大题,其本质都是在考查“结构决定性质,性质反映结构”这一核心思想。
常见官能团的结构与性质

根据常见试剂或特征现象
推断官能团种类

常见的有机反应类型


| 章节 | 内容 | 页码 | 章节 | 内容 | 页码 |
|---|---|---|---|---|---|
| 无机化学 | 化学实验基本方法 | -1 | 有机化学 | 有机化合物 | -43 |
| 物质的量 气体摩尔体积 | -3 | 烷烃 | -45 | ||
| 物质的量在化学实验中的应用 | -3 | 乙烯 | -52 | ||
| 物质的分类 | -4 | 烯烃 | -56 | ||
| 氧化还原反应 | -5 | 炔烃、炔烃 | -62 | ||
| 离子反应 | -6 | 苯及其同系物、芳香烃 | -66 | ||
| 钠及其氧化物 碱金属 | -7 | 石油 | -79 | ||
| 铝及其化合物 | -8 | 煤 | -81 | ||
| 铁及其化合物 | -9 | 烃的衍生物 | -83 | ||
| 用途广泛的金属材料 铜及其化合物 | -10 | 醇 | -88 | ||
| 无机非金属材料的主角 —— 硅 | -12 | 苯酚 | -98 | ||
| 富集在海水中的元素 —— 氯 | -13 | 羧酸 | -113 | ||
| 硫的氧化物和硫酸 | -14 | 酯 | -121 | ||
| 氮及其化合物 | -15 | 研究有机物的一般步骤和方法 | -125 | ||
| 原子结构 核外电子排布 | -17 | ||||
| 元素周期表和周期律 | -17 | ||||
| 化学键 | -18 | ||||
| 化学反应与能量变化 | -19 | ||||
| 化学反应速率 | -20 | ||||
| 化学平衡常数 | -22 | ||||
| 弱电解质的电离 | -23 | ||||
| 水的电离和溶液的酸碱性 | -23 | ||||
| 盐类的水解 | -25 | ||||
| 难溶电解质的溶解平衡 | -33 | ||||
| 电化学基础 | -38 |
金属 Na、K 起火:用沙土盖灭
酒精灯不慎碰倒起火:用湿抹布盖灭
浓碱液洒到皮肤上:用较多水冲洗,然后涂上硼酸溶液
浓硫酸溅到皮肤上:用布拭去,再用大量水冲洗,再涂上NaHCO₃溶液(若为大量浓硫酸溅到,先干布拭去,大量水冲洗,再用NaHCO₃溶液中和,再用水冲洗)
大量酸液洒在桌子上:用水冲洗,洗过的眼睛
不慎将酸溅到眼中:用水冲洗,边洗边眨眼睛
温度计水银球球不慎碰破:撒上硫粉
液体存放在细口瓶中,固体存放在广口瓶中。
碱性溶液、HF 不能用玻璃塞,强氧化性溶液不能用橡胶塞。
见光易分解的溶液存放在棕色试剂瓶中,并放在冷暗处,一般的存放在透明容器中。
少量 Na、K 保存在煤油中,少量白磷保存在水中,液溴用水封(取下层液体)。
加热制取气体,用排水法收集时,结束时不能先停止加热。
(2) 点燃 H₂、CH₄或 CO 时,应先检验气体的纯度。
(3) 涉及 H₂或 CO 的性质验证的综合实验装置加热时,应先排除装置中的空气。
(4) 浓 H₂SO₄稀释时,应将浓硫酸沿器壁慢慢注入水中并用玻璃棒不断搅拌。
若反过来,易发生暴沸溅出。
一贴:滤纸紧贴漏斗内壁
二低:滤纸低于漏斗边缘,液面低于滤纸边缘
三靠:烧杯紧靠玻璃棒,玻璃棒紧靠三层滤纸处,漏斗下端尖端紧靠烧杯内壁
① 玻璃棒的作用:搅拌,防止局部温度过高造成液体溅出
② 当有大量晶体析出时,停止加热,用余热蒸干液体

一、俗名………………………………………………3
二、颜色………………………………………………5
三、现象………………………………………………6
四、考试中经常用到的规律…………………………7
五、一些特殊的反应类型…………………………11
六、常见的重要氧化剂、还原剂…………………11
七、反应条件对氧化还原反应的影响……………12
八、离子共存问题……………………………………13
九、离子方程式判断常见错误及原因分析…………14
十、中学化学实验操作中的七原则………………16
十一、特殊试剂的存放和取用 10 例………………16
十二、中学化学中与 “0” 有关的实验问题 4 例及小数点问题…17
十三、能够做喷泉实验的气体……………………17
十四、比较金属性强弱的依据……………………17
十五、比较非金属性强弱的依据…………………18
十六、“10 电子”、“18 电子” 的微粒小结…………18
十七、微粒半径的比较……………………………19
十八、各种 “水” 汇集………………………………19
十九、具有漂白作用的物质………………………20
二十、各种 “气” 汇集………………………………20
二十一、滴加顺序不同,现象不同………………20
优秀的你值得更好的一切
各种苏打
纯碱、苏打、天然碱 :
小苏打: 大苏打:
各种石膏
石膏(生石膏): 熟石膏:
各种石灰
石灰石、大理石: 生石灰: 熟石灰、消石灰:
铁相关
绿矾: 磁铁矿: 黄铁矿、硫铁矿:
菱铁矿: 铁红、铁矿:
硫酸亚铁铵(淡蓝绿色): 溶于水后呈淡绿色
各种矾
胆矾、蓝矾: 明矾: 绿矾:
皓矾:
其他无机相关
莹石: 重晶石:(无毒) 水煤气: 和
芒硝:(缓泻剂) 漂白粉:、(混合物)
硅石、石英: 刚玉: 铜绿、孔雀石:
水玻璃、泡花碱、矿物胶: 赤铜矿: 尿素:
波尔多液: 和 玻璃的主要成分:、、
天然气、沼气、坑气(主要成分):
光化学烟雾: 在光照下产生的一种有毒气体
王水:浓与浓按体积比混合而成
铝热剂: 或其它氧化物
氢氟酸:—— 腐蚀玻璃